
Встановлено, що знизити ризики розвитку колібактеріозу в стаді можна шляхом формування у птиці ефективного захисту від хвороби Гамборо та імуносупресії
Імуносупресія та колібактеріоз

Встановлено, що знизити ризики розвитку колібактеріозу в стаді можна шляхом формування у птиці ефективного захисту від хвороби Гамборо та імуносупресії.
Розвиток птахівничої галузі та збільшення поголів’я птиці наразі відбувається швидкими темпами, що потребує постійного вдосконалення підходів вирощування, годівлі та профілактики захворювань. Однак значне концентрування птиці в пташнику на ряду з порушенням менеджменту та біобезпеки в господарстві значно підвищує ризики виникнення й поширення небезпечних патогенів. Часто вони мають резистентність до сучасних лікарських засобів і здатні уникати імунної відповіді через значну антигенну варіативність. Наприклад, бактерії E. coli, які є представником нормобіоти кишківника за набуття чинників вірулентності, а саме, ентеротоксинів, адгезинів, протектинів, гемолізинів, систем секреції, генів стійкості до антибіотиків, спричинюють колібактеріоз, який може проявлятися як колісептицемія, колігранульоматоз, синдром опухання голови, коліформний цельоліт, перитоніт, сальпінгіт, орхіт, омфаліт тощо.
КОЛІБАКТЕРІОЗ У ПТИЦІ
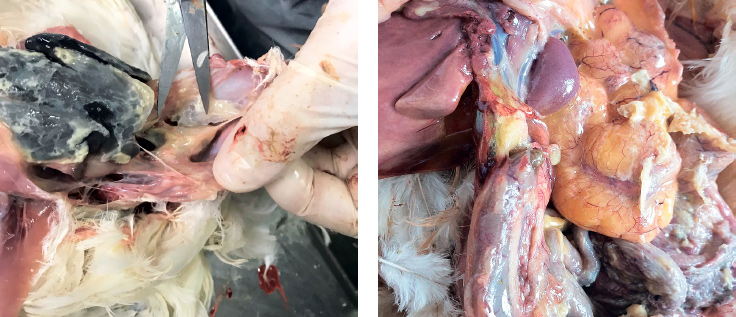
Більшість патогенних для птиці E. coli (APEC) належать до позакишкових патогенів, які призводять до появи системної чи генералізованої форми інфекції. До того ж патогенні ізоляти бактерій E. coli у птиці з імуносупресивним станом досить часто виступають саме вторинним чинником патологічного процесу, що сприяє розвитку бактеріальної інфекції.

Колібактеріоз є однією з основних причин смертності (до 20%) і захворюваності птиці, а також призводить до зниження виробництва м’яса птиці (зменшення живої ваги на 2%, погіршення коефіцієнта конверсії корму на 2,7%) і несучості (до 20%), зниження показників виводимості та збільшення вибраковування тушок (до 43%) на забої. Крім того, APEC відповідає за високу смертність (до 53,5%) курчат до 10 дня. Разом із витратами на лікування APEC обходиться птахівництву в сотні мільйонів доларів економічних збитків у всьому світі. У Сполучених Штатах було підраховано, що економічні збитки бройлерної промисловості можуть досягати до 40 млн доларів щорічно тільки через контамінацію тушок.
Безліч серотипів APEC були пов’язані з випадками колібактеріозу під час польових спалахів; однак три серотипи (O1, О2, О35, О78) є причиною більшості (понад 80%) випадків. APEC призводять до системних інфекцій у курей або як первинний патоген, або як вторинний чинник на тлі вірусних респіраторних (інфекційний бронхіт (IBV), хвороба Ньюкасла (NDV), пташиний грип (AIV)) та імуносупресивних хвороб (інфекційна бурсальна хвороба (IBD)), або впливу стрес-чинників (переущільнення, високий рівень пилу й аміаку). Відомо, що APEC можуть колонізувати шлунково-кишкові та дихальні шляхи курей, не спричиняючи захворювання, і як опортуністичний патоген змінювати локалізацію на позакишкову за наявності стресових чинників. Патогенні E. coli проникають через шлунково-кишковий тракт і дихальні шляхи у ділянках пошкодженого епітеліального шару, таким чином досягають кровотоку та внутрішніх органів. Кури заражаються через контаміновані корми та воду й можуть передавати патоген іншій птиці фекально-орально або аерозольним шляхом. Крім того, APEC можуть передаватися вертикально від інфікованих племінних стад через заражені яйця.
Останні дослідження вказують на те, що APEC (зокрема ізоляти, що належать до типів послідовності ST95 і ST131 або серогруп O1, O2 і O18) є потенційним зоонозним патогеном харчового походження, а також джерелом або резервуаром позакишкових інфекцій у людей. Зокрема, APEC мають генетичну подібність із позакишковими патогенними для людини бактеріями E. coli, а саме, уропатогенною кишковою паличкою (UPEC) і збудником неонатального менінгіту (NMEC). Крім того, патогенні для птиці E. coli здатні спричиняти інфекції сечовивідних шляхів і менінгіт на моделях мишей і щурів. До того ж виявлення APEC-специфічних плазмід ColV (коліцин V) в позакишкових ізолятах патогенних для людини свідчить про можливу зоонозну передачу саме від птиці. Таким чином, APEC є патогеном, важливим не лише для птахівництва, а й охорони здоров’я.
БОРОТЬБА З E. COLI
Бактерії E. coli належать до грамнегативних рухливих паличкоподібних мікроорганізмів, які здатні формувати капсулу та біоплівку, що значно ускладнює лікування та підготовку пташників. Інкубаційний період може становити від одного до кількох днів. Слід зазначити, що ці бактерії є досить стійкими до дезінфекційних засобів через наявність плазмід IncHI2, p-APEC-O1-R, IncF, pAPEC-O2-R тощо. Саме вони надають резистентність до телуриту калію, нітрату срібла, сульфату міді, четвертинних сполук амонію, хлориду бензалконію та навіть антибіотиків після перенесення плазміди до штаму-реципієнта шляхом кон’югації. Такі плазміди легко переносяться в інші APEC, коменсальні E. coli, Salmonella spp. та уропатогенні E. coli людини шляхом кон’югації, що вказує на еволюційну значущість цього процесу в появі резистентних штамів бактерій небезпечних для птиці й людини.
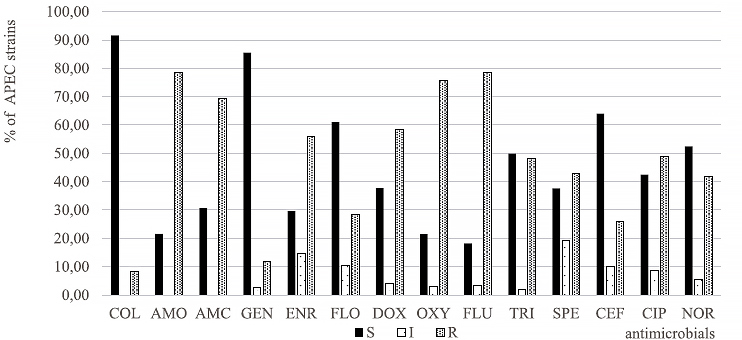
Для боротьби з колібактеріозом у курей часто використовують антибіотики різних класів і широкого спектра дії (тетрацикліни, сульфаніламіди, аміноглікозиди, феніколи, хіонолони). Проте підвищення стійкості APEC до різних класів антибіотиків, зокрема важливих для медицини β-лактамів, колістину, ципрофлоксацину, флорфеніколу, тетрациклінів та карбапенемів, говорить про появу небезпечних мультирезистентних штамів із відсутністю можливості лікування. За даними О. Нечипуренко, Д. Древаль та інших дослідників, понад 50% виділених APEC протягом 2015–2022 рр. в Україні були резистентними до амоксициліну, амоксиклаву, доксицикліну, оксітетрацикліну, флумеквіну, тріметоприму та спектиноміцину.
Крім того, не існує ефективної вакцини для захисту курей від бактерій APEC, що в основному пов’язано з різноманітністю серотипів і системним перебігом захворювання незалежно від віку птиці. Саме тому одним із підходів профілактики захворювання є контроль над імуносупресивними захворюваннями, а саме хворобою Гамборо. Це стало можливим завдяки застосуванню імунокомплексних вакцин (вакцинний вірус оточений антитілами), наприклад на основі вінтерфілд подібного штаму 1052.
Імунокомплекс (ІМК) об’єднує переваги живих і векторних вакцин, внаслідок застосування формується клітинний і гуморальний імунітет, а також інгібується зв’язування польового патогену з клітинами бурси, оскільки відповідні сайти зайнято вакцинним вірусом. ІМК є ефективним навіть за наявності материнських антитіл, бо після підшкірного введення він захоплюється дендритними клітинами, які беруть участь у представленні антигену через МНС-1 (клітинний імунітет) та МНС-2 (гуморальний імунітет), частина віріонів переходить у нативний стан, що знижує рівень материнських антитіл і стимулює реплікацію вакцинного вірусу. Крім того, після введення ІМК відбувається сильніша активація гермінативних центрів у селезінці та бурсі, порівнюючи з іншими вакцинами, через його транспортування безпосередньо в ці центри, що спричиняє індукцію В-лімфоцитів.
Антитіла для створення імунокомплексу отримують із SPF-яєць гіперімунізованих батьків, що дає можливість забезпечити їх надлишок, краще зв’язування та гомогенність імунокомплекса. Слід зазначити, що при виробництві проводять три етапи контролю якості продукції: вимірюють кількість вільних антитіл до і після зв’язування з вакцинним вірусом, крім того, визначають активність вірусних частинок (СID50) і титр вірусу (PU) в ІМК. Це гарантує рівень стабільної роботи вакцини.
Відповідно до даних Європейського бюро Фармакопеї, вакцинний вірус, штам 1052, не викликає загальну імуносупресію та здатен швидко колонізувати бурсу, що особливо важливо у формуванні захисту від хвороби Ньюкасла, інфекційного бронхіту, а також позитивно впливає на показники середньодобових приростів ваги.
Отже, формуючи ефективний захист від хвороби Гамборо й уникаючи імуносупресії, можливо значно знизити ризики розвитку колібактеріозу, що є основною причиною загибелі курчат як у бройлерному, так і яєчному виробництві.
Олексій Нечипуренко, канд. біол. наук, спеціаліст з технічної підтримки, Laboratorios Hipra, S.A.
Ольга Іващенко, канд. біол. наук, керівниця напряму птахівництво, Laboratorios Hipra, S.A.
Світлана Гаташ, спеціалістка з технічної підтримки, Laboratorios Hipra, S.A.






 Наше Птахівництво
Наше Птахівництво